4.腐食
腐食は、化学・生物学的作用により、外見や機能が損なわれた物体あるいはその状態のことです。金属は、周囲の環境(隣接している金属・気体など)と化学的あるいは電気化学的な反応を起こし、侵食されたりあるいは腐食生成物を生成したりします。表面的に「さび」が発生するだけにとどまらず、腐食により厚さが減少したり、孔が開いたり、隙間が出来たりすることも含みます。
金属の腐食は、酸化還元反応により表面の金属が、電子を失ってイオン化し金属面から脱落して行くことで進行します。生じたイオンは、多くの場合、酸素により、酸化物、水酸化物あるいは炭酸塩(緑青の場合)となり、表面に堆積します。金属イオンが酸化物に置き換わってゆく過程で、結晶構造や物性が著しく変化する場合も多くあります。一般的には、金属が腐食すると、形状ならびに強度が損なわれ、表面に錆が現れます。
金属表面は普通、1ミクロン以下の薄い酸化物で覆われています。金属表面はエネルギー的に不安定なため、大気中の酸素分子と反応して酸化物のバリアー層を形成します。無垢な金属表面は自然な状態では、ほとんど存在しません。表面に存在する酸化物バリアー層は、金属種類や環境、加工や異物付着などにより千差万別であり、表面の防腐食性も変わってきます。
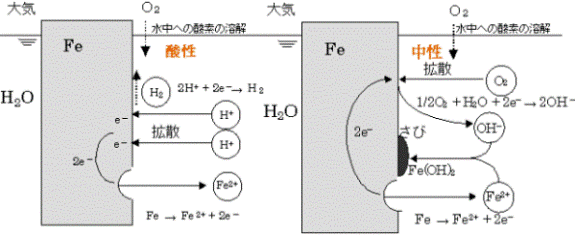
物理的あるいは化学的作用により金属表面の酸化物バリアー層が損なわれやすいと、バリアー層の剥離と表面の酸化は繰り返され、腐食面は金属内部に陥入します。特に水分と微量の酸の存在は、金属の腐食プロセスを加速させます。金属のイオン化傾向が水素イオン(H+)よりも大きければ、金属表面は容易にイオン化します。金属酸化物に水溶性があれば、それによってもバリアー層は剥離されます。バリアー層あるいはめっき面の点状の欠損から腐食が陥入する状態は孔食(点食、ピッティングコロージョン)と呼ばれています。ハロゲンイオン(主に塩素イオン、Cl-)の存在はピッティングコロージョンの引き金になることよくが知られています。一旦孔が腐食によって生成されると、金属表面は電気的・物理的に不均一となり、腐食を促進させる傾向があります。金属の腐食に必要なものは水と酸素で、(1)酸が水中で解離して生じる水素イオン(H+)か、(2)空気中から水に溶け込んだ溶存酸素により腐食が生じます。
日本付着生物学会が発足50周年を記念して編集した”付着生物のはなし/ 生態・防除・環境変動・人との関わり(朝倉書店2024.11)”に、生物の側から見た研究開発の現状と問題点が丁寧に解説されています。異なる分野の研究者達による、錆に対する異なった視点は、生活者としては”わが意を得たり”と言う内容もあり、また、溶接に関わる人間としては、意表を突かれる指摘もあります。若い研究者志望の方にはぜひ読んでいただきたい書籍です。
2016.3.17作成 2026.01.12改定